
- Зохиолч Miles Stephen stephen@answers-science.com.
- Public 2023-12-15 23:39.
- Хамгийн сүүлд өөрчлөгдсөн 2025-06-01 05:05.
хоёр
Эндээс ямар элементүүд Ауфбаугийн зарчмаас үл хамаарах зүйл вэ?
Жишээлбэл, рутений, родий, мөнгө, цагаан алт бүгд байдаг Ауфбаугийн зарчмаас үл хамаарах зүйл учир нь дүүрсэн эсвэл хагас дүүргэсэн дэд бүрхүүлүүд.
Дээрээс нь зэсийн электрон тохиргоо яагаад 1s22s22p63s23p63d94s2 биш харин 1s22s22p63s23p63d104s1 байдаг вэ? Дүүргэгдсэн дэд түвшин нь хагас дүүргэсэн дэд түвшнээс илүү тогтвортой байдаг. -ийн зохион байгуулалт электронууд ижил эргэх нь аль болох бага байна. 4s орбитал нь 3d орбиталаас өндөр энергитэй байдаг.
Мөн D блокийн элементүүдийн электрон тохиргоог хэрхэн бичих вэ?
Ерөнхийдөө, цахим тохиргоо Эдгээрийн элементүүд (n-1) г 1-10ns 1-2. (n-1) нь дотогшоо үлдэнэ г Нэгээс арван электронтой байж болох орбиталууд, захын ns орбитал нь нэг эсвэл хоёр электронтой байж болно. The г - блок s- ба p--ээр хүрээлэгдсэн дунд хэсгийг хамарна. блокууд үечилсэн хүснэгтэд.
Яагаад Cr болон Cu нь жигд бус тохиргоог харуулж байна вэ?
Үүнтэй ижил зүйл тохиолддог Cu . Бид чадна дотор нь хараарай Cu d дэд бүрхүүл нь 9 электронтой тул тогтвортой байхын тулд d дэд бүрхүүлд 1 электрон шаардлагатай тул s дэд бүрхүүлээс 1 электрон авна. Cu шинэ электрон төхөөрөмждөө тогтвортой байх болно тохиргоо . Тиймээс, Cr ба Cu байна онцгой гэж нэрлэдэг тохиргоо.
Зөвлөмж болгож буй:
Протоны масс ба электроны массын хооронд ямар ялгаа байдаг вэ?
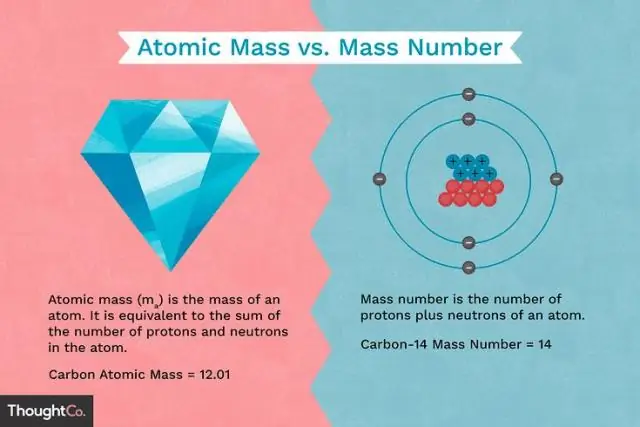
Протон ба нейтрон нь ойролцоогоор ижил масстай боловч хоёулаа электроноос хамаагүй их масстай (электроноос ойролцоогоор 2000 дахин их). Протон дээрх эерэг цэнэг нь электрон дээрх сөрөг цэнэгийн хэмжээтэй тэнцүү байна
Архебактерийн хаант улсад хэдэн зүйл байдаг вэ?

Археагийн 209 зүйл нь 63 төрөлд хуваагддаг бөгөөд үүнээс 24 нь монотип (угийн зөвхөн нэг зүйл байдаг гэсэн үг). Архейг Euryarchaeota, Crenarchaeota, Korarchaeota гэсэн 3 үндсэн бүлэгт хуваадаг
Стандарт температур, даралт гэж юу вэ Стандарт яагаад шаардлагатай вэ?

Температур, даралтаас ихээхэн хамаардаг шингэний урсгалын хурд, шингэн ба хийн эзэлхүүний илэрхийлэлд стандарт жишиг нөхцөл чухал байдаг. Тооцоололд стандарт төлөвийн нөхцлийг ашиглах үед STP-ийг ихэвчлэн ашигладаг
Стандарт нэмэх арга нь яагаад илүү үнэн зөв байдаг вэ?

Хэрэв дээж нь матрицын нөлөө үзүүлдэг бол стандарт нэмэлт процедур нь стандарт муруйг ашиглахаас илүү нарийвчлалтай дээж дэх задлан шинжлэлийн агууламжийг хэмжих боломжийг олгоно. Нэмэлт аналитик нь дээжинд байгаа зүйлтэй ижил матрицын нөлөөг мэдэрдэг гэсэн таамаглал юм
Нүүрстөрөгчийн огноотой байхын тулд ямар нэгэн зүйл хэдэн настай байх ёстой вэ?

Нүүрстөрөгчийн 14-ийн болзоо нь 50,000 орчим жилийн настай биологийн гаралтай зарим археологийн олдворуудын насыг тодорхойлох арга юм. Хүн төрөлхтний үйл ажиллагаанаас харьцангуй ойрын үед бий болсон чулуун чулуу, даавуу, мод, ургамлын утас зэрэг зүйлсийг болзоход ашигладаг
