
- Зохиолч Miles Stephen stephen@answers-science.com.
- Public 2023-12-15 23:39.
- Хамгийн сүүлд өөрчлөгдсөн 2025-01-22 17:05.
хлор изотоп 18 нейтронтой бол элбэг дэлбэг 0.7577, массын тоо 35 аму байна. Тооцоолохын тулд дундаж атомын масс, бутархайг тус бүрийн массын тоогоор үржүүлнэ изотоп , дараа нь тэдгээрийг хамтад нь нэмнэ.
Үүний нэгэн адил элементийн бүх изотопын жигнэсэн дундаж нь хэд вэ?
Янз бүрийн массыг ашиглах изотопууд мөн тус бүр нь хэр их байдаг изотоп нь бид олж чадна дундаж атомын масс бүрэлдэхүүн . Атомын масс бүрэлдэхүүн нь жигнэсэн дундаж байгалийн гаралтай дээж дэх атомын масс бүрэлдэхүүн . Атомын массыг ихэвчлэн атомын массын нэгжээр илэрхийлдэг.
1 аму ямар масстай вэ? Атомын массын нэгжийг (AMU эсвэл amu гэсэн тэмдэглэгээ) нүүрстөрөгч-12-ын атомын массын яг 1/12 гэж тодорхойлдог. Нүүрстөрөгч-12 (C-12) атом нь зургаатай протонууд ба зургаа нейтрон түүний цөмд. Тодорхой бус утгаараа нэг AMU нь дундаж юм протон амрах масс ба нейтрон амрах масс.
Хоёрдугаарт, атомын массыг ашиглан элбэг дэлбэг хувийг хэрхэн тооцоолох вэ?
Тус бүрийг өөрчлөх элбэг дэлбэг хувь 100-д хувааж аравтын бутархай хэлбэрт шилжүүлнэ. Энэ утгыг -аар үржүүлнэ атомын масс тэр изотопын. Дундажийг авахын тулд изотоп тус бүрийг нэм атомын масс.
Атомын масс ба атомын жин хоёрын ялгаа юу вэ?
Атомын масс (ма) нь масс нэг атом . Ганц бие атом тодорхой тооны протон ба нейтронтой тул масс Энэ нь тодорхойгүй (өөрчлөхгүй) бөгөөд протон ба нейтроны тооны нийлбэр юм. атом дахь . Атомын жин -ийн жигнэсэн дундаж юм масс бүхнээс атомууд изотопын элбэг дэлбэг байдал дээр үндэслэсэн элементийн.
Зөвлөмж болгож буй:
NaOH-ийн молекул жинг хэрхэн олох вэ?

Хариулт ба тайлбар: Натрийн гидроксидын молийн масс нь 39.997 г/моль. Молийн массыг тодорхойлохын тулд атомын массыг томьёоны атомын тоогоор үржүүлнэ
Хоёр хурдтай дундаж хурдыг хэрхэн олох вэ?
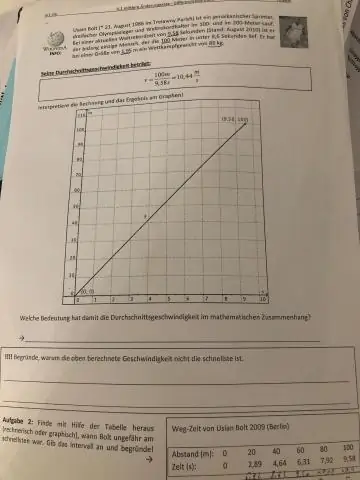
Эхний болон эцсийн хурдны нийлбэрийг 2-т хувааж дундажийг олно. Дундаж хурдны тооцоолуур нь дундаж хурд (v) нь эцсийн хурд (v) ба анхны хурд (u) нийлбэрийг 2-т хуваасан томъёог ашигладаг
Шингэн хольцын хувийн жинг хэрхэн олох вэ?

Одоо нийт нягтыг усны нягтаар хувааж, хольцын SG-ийг авна. Хамгийн их нягтралтай шингэн гэж юу вэ? Тэнцүү эзэлхүүнтэй хоёр бодис холилдоход хольцын хувийн жин 4 байна. p нягттай шингэний масс нь өөр нягттай3p шингэнтэй тэнцүү масстай холилдоно
Дундаж утгыг өгвөл алга болсон тоог хэрхэн олох вэ?

Олон тооны тооны дундаж нь эдгээр тоонуудын дундаж юм. Та тоонуудын багцыг нэмж, хэдэн тоо өгөгдсөнийг хуваах замаар сэдвийг олох боломжтой. Хэрэв танд санаа өгөөд, уг багцаас дутуу тоог олохыг хүсвэл энгийн тэгшитгэл ашиглана уу
H2so4-ийн молекул жинг хэрхэн олох вэ?

H2SO4-ийн молийн массыг бүрдүүлж буй бүх элементийн молийн массыг нэмж тооцоолж болно. H(x2)-ийн моляр масс+Хүхрийн(х1) молийн масс+Хүчилтөрөгчийн моляр масс(х4). =>98г/моль
