- Зохиолч Miles Stephen stephen@answers-science.com.
- Public 2023-12-15 23:39.
- Хамгийн сүүлд өөрчлөгдсөн 2025-01-22 17:05.
% цэвэр ариун байдал = олж авсан цэвэр бодисын г ÷ gof өгсөн дээж ×100. Цэвэр байдлын хувь бодис байж болно тооцоолсон цэвэр химийн бодисын массыг дээжийн нийт массад хувааж, дараа нь энэ тоог 100-аар үржүүлнэ.
Эндээс харахад цэвэршилтийн хувь нь гарцын хувьтай ижил байна уу?
Хувийн өгөөж & Цэвэр ариун байдал . Эдгээр хичээлүүдэд бид яаж хийхийг авч үзэх болно тооцоолох нь хувийн ашиг урвалаас болон цэвэршилт хувь олж авсан бүтээгдэхүүний. The ургац нь урвалаас олж авах бүтээгдэхүүний хэмжээ юм. Манайх бордоо, будаг хийдэг үйлдвэртэй гэж бодъё.
Дараа нь асуулт бол цэвэр байдал ба шинжилгээ хоёрын ялгаа юу вэ? Үндсэн шинжилгээний хоорондох ялгаа болон цэвэр ариун байдал энэ нь а шинжилгээ үндсэн бүрэлдэхүүн хэсгүүдийн аль нэгийг тодорхойлох явдал юм дотор харин дээж цэвэр ариун байдал хольцыг тодорхойлох явдал юм дотор дээж. Шинжилгээ болон цэвэр ариун байдал нь дээжийн бүрэлдэхүүн хэсгүүдийг тодорхойлоход ашигладаг хоёр төрлийн хэмжилт юм.
Мөн та давсны цэвэр байдлыг хэрхэн шалгах вэ?
Нийтлэг давс , нэгдэл бүрийн моль нь 1-ээс 1 харьцаатай байна. Цэвэр байдал нийтлэг зүйлийн давс Дээжийн молийн масс, элемент бүрийн темоляр масс, найрлагын хувийн стандарт утгуудын мэдлэгээр нэгдлийг тодорхойлж болно. давс хамгийн цэвэрхэн.
Та цэвэр бодисыг хэрхэн тодорхойлох вэ?
Цэвэр бодисууд гэж тодорхойлсон бодисууд зөвхөн нэг төрлийн атом эсвэл молекулаас бүрддэг. Цэвэр ариун байдал нь а бодис нь өгөгдсөн хэмжээг илэрхийлэх хэмжүүр юм бодис байна цэвэр . Физик шинж чанар нь a цэвэр бодис сайн тодорхойлогдсон хайлах болон буцлах цэгүүдийг багтаана.
Зөвлөмж болгож буй:
Хлорын элбэг хувийг хэрхэн тооцоолох вэ?

18 нейтронтой хлорын изотоп нь 0.7577 элбэг, массын тоо 35 аму байна. Дундаж атомын массыг тооцоолохын тулд изотоп тус бүрийн бутархайг массын тоогоор үржүүлж, дараа нь тэдгээрийг нэгтгэнэ
KClO3 дахь хүчилтөрөгчийн онолын хувийг хэрхэн олох вэ?

KClO3-ийн дээж дэх хүчилтөрөгчийн туршилтын хувийг энэ тэгшитгэлийг ашиглан тооцоолно. Туршилтын % хүчилтөрөгч = Алдагдсан хүчилтөрөгчийн масс x 100 KClO3-ын масс Калийн хлорат дахь хүчилтөрөгчийн %-ийн онолын утгыг молийн масс = 122.6 г/моль KClO3 томъёогоор тооцоолно
Эмпирик дүрмийг ашиглан ойролцоогоор хувийг хэрхэн олох вэ?

X = 9-ээс x = 13 хүртэлх муруйн доорх талбайг олох. Эмпирик дүрэм буюу 68-95-99.7% Дүрэм нь нэг стандарт хазайлт (68%), хоёр стандарт хазайлт (95%) дотор багтах өгөгдлийн ойролцоогоор хувийг өгдөг. , мөн дундажийн гурван стандарт хазайлт (99.7%) байна
Хүчдэлийн уналтын хувийг хэрхэн тооцоолох вэ?

Хүчдэлийн уналтыг тооцоолохын тулд: Ампер-футыг авахын тулд ампер дахь гүйдлийг хэлхээний уртаар футаар үржүүлнэ. Хэлхээний урт нь хэлхээний эхлэл цэгээс ачааллын төгсгөл хүртэлх зай юм. 100-д хуваана. Хүснэгтэнд тохирох хүчдэлийн уналтын утгыг үржүүлнэ. Үр дүн нь хүчдэлийн уналт юм
Молярын хувийг хэрхэн тооцоолох вэ?
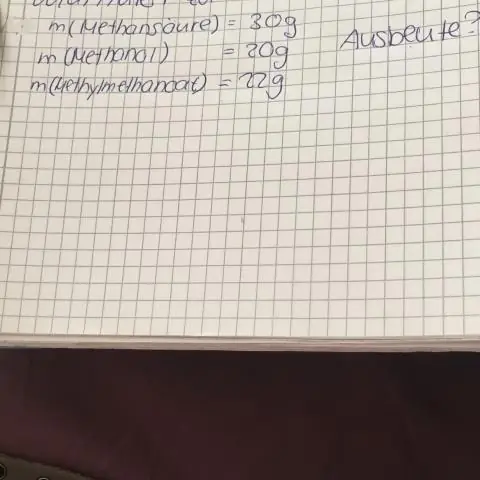
Моль ба молийн уусмал (нэгж = M = моль/л) Процент уусмал (% = зуун тутамд хэсэг буюу грамм/100 мл) % уусмалаас молярьд шилжүүлэхийн тулд % уусмалыг 10-аар үржүүлж, уусмалын грамм/л хувийг илэрхийлнэ. томъёоны жингээр
